Reaksi redoks merupakan reaksi kimia yang melibatkan perpindahan elektron antarzat. Dalam setiap reaksi redoks selalu terjadi oksidasi dan reduksi secara bersamaan, sehingga keduanya tidak dapat dipisahkan.
Oksidasi didefinisikan sebagai peristiwa pelepasan elektron atau peningkatan bilangan oksidasi, sedangkan reduksi adalah penerimaan elektron atau penurunan bilangan oksidasi. Konsep bilangan oksidasi digunakan untuk mempermudah identifikasi proses redoks.
Reaksi redoks banyak terjadi dalam kehidupan sehari-hari, seperti proses pernapasan, pembakaran bahan bakar, dan fotosintesis. Tanpa disadari, hampir semua proses energi melibatkan reaksi redoks.
Elektrokimia merupakan cabang kimia yang mempelajari hubungan antara reaksi redoks dan energi listrik. Pada elektrokimia, energi kimia dapat diubah menjadi energi listrik atau sebaliknya.
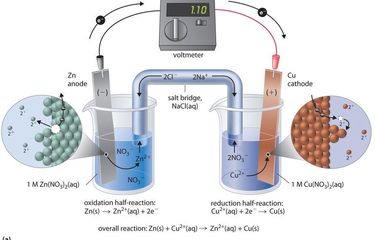
Sel volta atau sel galvanik adalah alat yang mengubah energi kimia menjadi energi listrik melalui reaksi redoks spontan. Sel ini terdiri dari dua elektroda yang berbeda potensial dan dihubungkan oleh jembatan garam.
Perbedaan potensial antara kedua elektroda menghasilkan arus listrik. Prinsip kerja sel volta dimanfaatkan dalam berbagai jenis baterai yang digunakan sehari-hari.
Elektrolisis adalah proses penguraian zat dengan bantuan arus listrik. Berbeda dengan sel volta, reaksi redoks pada elektrolisis bersifat tidak spontan dan memerlukan energi listrik dari luar.
Proses elektrolisis banyak digunakan dalam industri, seperti pemurnian logam, pelapisan logam, dan produksi zat kimia tertentu. Elektrolisis juga berperan penting dalam teknologi modern.
Korosi merupakan proses redoks yang merugikan karena menyebabkan kerusakan pada logam, terutama besi. Korosi terjadi akibat reaksi logam dengan oksigen dan air di lingkungan.
Upaya pencegahan korosi dapat dilakukan melalui pelapisan, penggunaan logam pelindung, dan proteksi katodik. Pemahaman redoks dan elektrokimia membantu mengembangkan teknologi yang lebih tahan lama dan efisien.